PERISO- Pompa diamagnetyczna CTU MEGA 20 w leczeniu pacjenta z mieszanym owrzodzeniem stopy
Streszczenie: Owrzodzenia kończyn dolnych są związane z rosnącą częstością występowania oraz znaczącymi kosztami ekonomicznymi i społecznymi. Do tej pory nie ma wysokiej jakości dowodów związanych z optymalnym algorytmem leczenia. Potrzebne jest podejście multimodalne, szczególnie u pacjentów z chorobami współistniejącymi i wielochorobowością. W niniejszym dokumencie opisano przypadek 94-letniej kobiety rasy kaukaskiej z chorobami współistniejącymi i politerapią, która została przyjęta na naszą obserwację z powodu przewlekłego bolesnego owrzodzenia mieszanego kostki w wywiadzie (1 rok). Po ocenie klinicznej zastosowano u niej terapię przeciwbólową dwa razy dziennie oraz cotygodniową terapię diamagnetyczną i leczenie miejscowe. Podczas badania klinicznego udokumentowaliśmy statystycznie istotną poprawę zarówno w zakresie bólu (wynik w skali VAS z 8 do 2 p < 0,01), jak i owrzodzenia stopy (zmniejszenie powierzchni z 6 cm × 4 cm do 2 cm × 2 cm, p < 0,01) w szóstym tygodniu leczenia skojarzonego. Owrzodzenie całkowicie zagoiło się w dziewiątym tygodniu. Jest to pierwsze badanie dokumentujące wpływ terapii diamagnetycznej jako terapii dodatkowej w leczeniu gojenia się ran. Podsumowując, nawet jeśli nadal brakuje wysokiej jakości dowodów, terapia diamagnetyczna może stanowić interesującą opcję jako dodatkowe leczenie owrzodzeń.
Słowa kluczowe: terapia diamagnetyczna; owrzodzenie mieszane; stopa; leczenie
1. Wprowadzenie
Owrzodzenia kończyn dolnych, które są głównie reprezentowane przez owrzodzenia żylne kończyn dolnych, owrzodzenia stopy cukrzycowej, owrzodzenia uciskowe i owrzodzenia tętnicze, dotykają do 49 milionów ludzi rocznie na całym świecie, z oczekiwanym dalszym wzrostem częstości występowania [1].
Owrzodzenia stóp wiążą się zarówno z obciążeniami ekonomicznymi (wysokie koszty leczenia ran i długi czas gojenia), jak i społecznymi (zachorowalność, wysokie ryzyko powikłań oraz wpływ na jakość życia pacjentów i krewnych) [2]. Leczenie ran przewlekłych obejmuje kilka podejść związanych z chorobą podstawową (np. terapię uciskową i odciążenie dotkniętego obszaru) [3], a zgodnie z metodą TIME (oczyszczanie tkanek, kontrola zakażeń, nierównowaga wilgotności i rozwój krawędzi) [4] stosuje się podejście multimodalne [1]. Nawet jeśli w leczeniu owrzodzeń stóp można stosować kilka związków [5-7], brakuje dowodów wysokiej jakości [8]; w związku z tym można by zastosować nowe strategie terapeutyczne w celu poprawy pomocy klinicznej i zmniejszenia kosztów społeczno-ekonomicznych.
Szczególne zainteresowanie wzbudziło wykorzystanie pól magnetycznych (MF) jako nieinwazyjnej i bezpiecznej opcji fizykoterapeutycznej w łagodzeniu bólu i naprawie tkanek.
Pola magnetyczne mogą wpływać na funkcje i aktywność komórek (np. tworzenie tkanek, migrację komórek, proliferację i adhezję), a tym samym mogą być korzystne dla gojenia się ran [9-14].
W odniesieniu do intensywności i kierunku, można je sklasyfikować jako statyczne MF i dynamiczne MF. Dynamiczne MF obejmują impulsowe pola elektromagnetyczne (PEMF), zwykle pola o niskiej częstotliwości o różnej intensywności wytwarzane przez prąd pulsacyjny [9]. Pulsacyjne pola magnetyczne o niskiej intensywności i częstotliwości (LI-LF-PEMF) są skuteczne w leczeniu zaburzeń układu mięśniowo-szkieletowego i innych patologii. Jednak impulsowe pola elektromagnetyczne o wysokiej intensywności i niskiej częstotliwości (HI-LF-PEMF) również aktywują efekty biologiczne przyspieszające molekularnie i odpychające wodę (diamagnetyczne), stąd neologizm Diamagnetic Therapy lub Diamagneto therapy [15,16].
Opisujemy przypadek 94-letniej kobiety rasy kaukaskiej, u której po raz pierwszy zastosowano terapię diamagnetyczną jako leczenie uzupełniające w gojeniu ran.
1. Prezentacja przypadku
94-letnia pacjentka rasy kaukaskiej (waga 75 kg, wzrost 167 cm, BMI 26,9) zgłosiła się do nas na wózku inwalidzkim z powodu silnego bólu owrzodzenia stopy.
Ocena kliniczna udokumentowała, że była zorientowana przestrzenno-czasowo i współpracowała.
Jej historia medyczna ujawniła, że 10 lat temu była dotknięta kilkoma chorobami ogólnoustrojowymi, choroby wymagające politerapii (Tabela 1).
Tabela 1. Charakterystyka kliniczna pacjentki.
Wiek, lata 94
Płeć Kobieta
Waga, kg 75
Wzrost, cm 167
BMI 26,9
Zaprzestanie palenia 20 lat temu
Wcześniejsza operacja artroprotezy prawego kolana Alergia na leki Diklofenak (skierowany)
Choroby współistniejące i codzienne leczenie farmakologiczne
Astmatyczne zapalenie oskrzeli : brane leki: Salmeterol 50 mcg plus flutikazon 100 mcg bid Tiotropium 18 mcg qd Tlenoterapia 3 lt qd
Choroby sercowo-naczyniowe i mózgowo-naczyniowe :Kwas acetylosalicylowy100 mg qd, Klopidogrel 75 mg/d Losartan 50 mg plus hydrochlorotiazyd 12,5 mg na dobę
Choroba refluksowa przełyku: Pantoprazol 20 mg/d Hiperurykemia Allopurynol 300 mg/d
Reumatoidalne zapalenie stawów (nieudokumentowane) Deksametazon 4 mg/.
Około rok temu rozwinęło się u niej owrzodzenie kostki stopy, które nie reagowało na nieokreślone leczenie miejscowe antybiotykami i kremami zabliźniającymi. Owrzodzenie pogorszyło jej jakość życia, ograniczając możliwości zarówno wychodzenia z domu, jak i stania. Zaprzeczyła wcześniejszej historii podobnych ran lub znanej historii choroby naczyń obwodowych lub urazu stopy. Zaprzeczyła również używaniu alkoholu, ale ujawniła wcześniejsze uzależnienie od nikotyny, które ustało około 20 lat temu.
Podczas badania klinicznego udokumentowano objawy zapalenia wielostawowego, z funkcjonalnym ograniczeniem kończyn górnych i owrzodzeniem (6,4 cm) na lewym kostce bocznej pokrytym strupem, z lekko podważonymi i rumieniowymi granicami. Powierzchnię owrzodzenia oceniono za pomocą linijki, podając największą długość i prostopadłą największą szerokość. Wykryto również obrzęk i przebarwienia wokół rany (patrz rysunek 1).
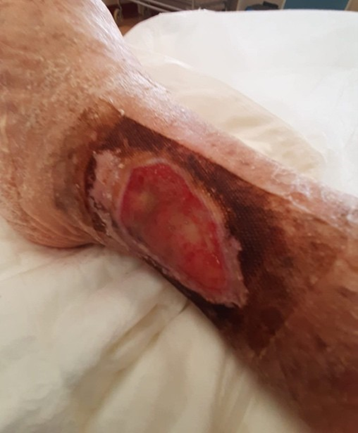
Rysunek 1. Wrzód na początku badania.
Trofizm skóry był zachowany i nie było żylaków. Lewa noga była cieplejsza niż prawa, ale badanie kliniczne wykluczyło infekcję na poziomie owrzodzenia. Pulsacje kończyn dolnych były słabo wyczuwalne; w związku z tym wskaźnik kostka ramię (ABI) wynosił 0,7, ujawniając umiarkowaną chorobę tętnic obwodowych.
Ocena bólu udokumentowała silny ból (wynik 8 w wizualnej skali analogowej (VAS)) z komponentem nocyceptywnym i wykluczyła obecność allodynii lub bólu neuropatycznego. Upośledzona jakość życia została oceniona za pomocą włoskiej wersji kwestionariusza SF-36 [17], który wykazał niskie wyniki głównie w zakresie bólu ciała, ogólnego stanu zdrowia oraz domen funkcjonowania fizycznego i społecznego.
Konsultacje z chirurgami naczyniowymi potwierdziły rozpoznanie mieszanego owrzodzenia żylno-tętniczego, ale według oceny klinicznej nie było wskazań do rewaskularyzacji tętnic.
Leczenie rany zalecono zgodnie ze współistniejącymi chorobami i politerapią. W związku z tym pacjent rozpoczął i) leczenie doustne - oksykodon w dawce 5 mg plus paracetamol w dawce 325 mg, ze stopniowym odstawianiem steroidoterapii; ii) cotygodniowe leczenie miejscowe - oczyszczenie rany, zaawansowane leki z idrokoloidem i bandażowanie z obniżonym poziomem ciśnienia (tj. 23-30 mmHg). Przed rozpoczęciem każdego cotygodniowego leczenia miejscowego oceniano powierzchnię owrzodzenia i wykonywano zdjęcie. Aby skrócić czas naprawy rany, rozpoczęto również terapię diamagnetyczną.
Protokół terapii diamagnetycznej
Sesja terapii diamagnetycznej była wykonywana raz w tygodniu. Zaplanowano protokół obejmujący co najmniej 10 sesji. Specyfikacje techniczne interwencji zostały ustalone poprzez połączenie wstępnie określonych protokołów producenta z doświadczeniem klinicznym pracowników służby zdrowia. Liczbę sesji można było rozszerzyć/przedłużyć w zależności od odpowiedzi klinicznej. Każda sesja terapeutyczna trwała 25 minut (ruchy płynów: Intra L-Extra H przez 10 min; endogenna biostymulacja: błona komórkowa przez 15 min). Podczas każdej interwencji pacjent znajdował się w pozycji siedzącej z podudziem i stopą podpartą za pomocą stojaka na stopy. Zastosowano terapię diamagnetyczną (pompa diamagnetyczna CTU MEGA 20®-Periso SA. Pazzallo-Szwajcaria) o częstotliwości 5 Hz, z gęstością strumienia magnetycznego 86 mT w miejscu leczenia (mierzoną na osi solenoidu).
1. Wyniki
Protokół leczenia skojarzonego spowodował statystycznie istotną poprawę zarówno w zakresie bólu (wynik w skali VAS z 8 do 2, p < 0,01), jak i owrzodzenia stopy (zmniejszenie powierzchni z 6 cm do 2 cm) 4 cm do 2 cm 2 cm, p < 0,01) po sześciu tygodniach leczenia, a następnie całkowite wyleczenie owrzodzenia (patrz rysunek 2). Miejscowe interwencje, w tym protokół diamagnetyczny, przerwano w dziewiątym tygodniu leczenia (dziewiąta sesja nie została wykonana, ponieważ wrzód już się zagoił). Leczenie farmakologiczne było kontynuowane ze względu na korzyści zgłaszane również w przypadku bólu związanego z zapaleniem wielostawowym. Pacjentka stwierdziła poprawę jakości życia, ocenianą za pomocą kwestionariusza SF-36, ujawniając, że była w stanie chodzić bez wsparcia. Rzeczywiście, odnotowano wyższe wyniki w domenach najbardziej dotkniętych na początku badania (ból ciała, ogólny stan zdrowia oraz funkcjonowanie fizyczne i społeczne). Nie zgłoszono żadnych zdarzeń niepożądanych związanych zarówno z leczeniem farmakologicznym, jak i niefarmakologicznym.
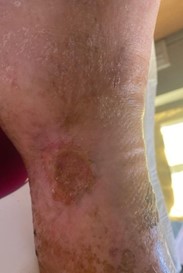
Rysunek 2. Wrzód w dziewiątym tygodniu leczenia.
1. Omówienie i wnioski
W niniejszym opisie przypadku udokumentowaliśmy pierwsze dodatkowe zastosowanie terapii diamagnetycznej w leczeniu mieszanego owrzodzenia stopy u starszej kobiety. Rana mieszana stanowi wyzwanie dla klinicystów, ponieważ nadal nie ma optymalnego algorytmu leczenia [18]. Co więcej, postępowanie kliniczne u starszych pacjentów jest dodatkowo komplikowane zarówno przez choroby współistniejące, jak i politerapię, co może zmniejszać przestrzeganie zaleceń terapeutycznych i zwiększać ryzyko interakcji lekowych i działań niepożądanych [19,20]. Biorąc pod uwagę te czynniki, nasza pacjentka była leczona przez rok miejscowo bez poprawy klinicznej. Po tym okresie zgłosiła się do nas, gdzie lekarze specjalizujący się w farmakologii klinicznej i chirurgii naczyniowej zasugerowali leczenie skojarzone. Wcześniejsze prace dokumentowały, że pacjenci z mieszanymi owrzodzeniami powinni być leczeni tradycyjnymi metodami lub nowymi opatrunkami biologicznymi [5,18]. Terapia uciskowa zwiększa przepływ żylny i drenaż limfatyczny oraz nasila fibrynolizę, poprawiając gojenie się owrzodzeń i zmniejszając częstość ich nawrotów [21]. Można ją jednak wykonywać tylko u pacjentów z ABI > 0,5 i bezwzględnym ciśnieniem w kostce > 60 mmHg [22]. Inne metody leczenia uzupełniającego, takie jak tlenoterapia hiperbaryczna, wykazały korzyści w badaniach krótkoterminowych, ale ich dostępność i koszty ograniczają ich stosowanie [23].
U naszego pacjenta operacja naczyniowa wykluczyła możliwość zabiegu chirurgicznego, dlatego rozpoczęto leczenie farmakologiczne za pomocą terapii diamagnetycznej, uzyskując szybką poprawę zarówno w zakresie bólu, jak i owrzodzenia stopy.
Pola magnetyczne, które są skuteczne w łagodzeniu bólu, mogą mieć potencjalne zastosowanie w ranach przewlekłych, ponieważ wydają się wpływać na wszystkie składniki procesu gojenia (np. fibrynę, płytki krwi, fibroblasty i czynniki wzrostu) [9,24]. Diamagnetyzm jest słabą właściwością magnetyczną materii, a jego ekspresja wymaga wysokich wartości MF, aby wykorzystać właściwości diamagnetyczne tkanek biologicznych, podobnie jak w przypadku innych form stymulacji elektromagnetycznej [25]. W tym opisie przypadku efekt diamagnetyczny był wywierany przez HI-LF PEMF.
Zaproponowano kilka mechanizmów wyjaśniających, dlaczego PEMF może skrócić czas gojenia się ran. Dane przedkliniczne pokazują, że PEMF może stymulować rozszerzenie naczyń krwionośnych, zwiększając przepływ krwi w naczyniach włosowatych skóry i perfuzję narządów, zmniejszając obrzęk tkanek miękkich i zwiększając aktywność metaboliczną [26,27]. Poprawa perfuzji krwi w tkankach stymulowanych magnetycznie jest mechanizmem stymulującym efekty w procesie regeneracji, skutkującym zarówno przyspieszoną proliferacją komórek, jak i hamowaniem stanu zapalnego [28]. Lee i wsp. [29] donieśli, że pola elektryczne i magnetyczne mogą modulować zarówno migrację komórek naprawczych, jak i aktywność kanałów jonowych w obszarze rany, a aktywność kanałów jonowych jest zaangażowana w gojenie się ran. Uznaliśmy, że leczenie polami magnetycznymi jest przydatne do przyspieszenia regeneracji tylko w przypadku braku fizjologicznego prądu elektrycznego lub aktywności biologicznej w procesie odbudowy.
Sygnały elektryczne generowane przez PEMF mogą oddziaływać na uszkodzone błony komórkowe, powodując zmniejszenie stanu zapalnego, wzrost liczby fibroblastów i makrofagów w owrzodzeniu oraz zwiększone odkładanie fibryny [30]. Markoll i wsp. wykazali spadek metaloproteaz macierzy (MMP) i wzrost tkankowego inhibitora MMP (TIMP) pod wpływem impulsowego pola magnetycznego [31]. Składniki te odgrywają rolę w patogenezie i przebudowie wrzodów [32]. PEMF może również wywoływać ich działanie, zmniejszając produkcję reaktywnych form tlenu (ROS) [33,34].
Dostępnych jest kilka niepotwierdzonych danych na temat korzystnych właściwości terapii elektromagnetycznej na rany skóry, ale nie są one rozstrzygające. Impulsowe pola magnetyczne przyspieszają gojenie się ran u szczurów: Strauch i wsp. opisali wzrost wytrzymałości rany na rozciąganie 21 dni po zranieniu [35]. Pola elektromagnetyczne wykazały pewien efekt w modulacji ran szkaplerza sztucznie wykonanych na zwierzętach: aplikacja bez modulacji częstotliwości była skuteczna w zmniejszaniu wysięku zapalnego [36].
W poprzednim badaniu z podwójnie ślepą próbą Ieran i wsp. [37] ocenili u 20 pacjentów wpływ pola elektromagnetycznego na gojenie się owrzodzeń żylnych, dokumentując, że w odniesieniu do placebo pole elektromagnetyczne jest w stanie poprawić objawy kliniczne, obniżając wskaźnik nawrotów owrzodzeń (p < 0,02).
Zgodnie z tym, w prospektywnym, randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu, Stiller i wsp. [38] ocenili wpływ pulsacyjnej elektromagnetycznej terapii owrzodzeń kończyn (PELUT) na gojenie się opornych, żylnych owrzodzeń nóg i wykazali, że PELUT wywołał znaczące zmniejszenie głębokości rany (p < 0,04) i nasilenia bólu (p < 0,04) w odniesieniu do grupy otrzymującej placebo. Kenkre i wsp. zrekrutowali dziewiętnastu pacjentów i zastosowali napromienianie o różnej częstotliwości (600 Hz i 800 Hz) w porównaniu z placebo. Pacjenci leczeni PEMF wykazali poprawę w zakresie kontroli bólu i wielkości owrzodzenia, terapia 800 Hz wydawała się być bardziej skuteczna niż 600 Hz lub placebo, a 68% pacjentów doświadczyło zdarzeń niepożądanych: bólu głowy (tylko grupa leczona), uczucia gorąca, mrowienia i mrowienia (grupy placebo i leczona) [39].
Istotną kwestią jest brak standaryzacji urządzeń PEMF pod względem typu, czasu trwania, częstotliwości oraz intensywności i długości ekspozycji [30]. Gordon opisał wzrost czasu (dB/dt) jako krytyczny czynnik determinujący skuteczność tego rodzaju leczenia, wywierający istotny wpływ na aktywację genów odbudowy [33]. Terapia polem magnetycznym powinna być dostarczana w dawkach podobnych do leku [9], dlatego lekarze powinni rozwinąć umiejętność dostosowywania odpowiedniego protokołu do patologii i cech pacjentów. Pomimo obecności efektów naczyniowych wspierających ich stosowanie [9,26,27,29], nie było danych dotyczących pacjentów cierpiących na
Chociaż w literaturze brakuje wysokiej jakości dowodów dotyczących PEMF w leczeniu owrzodzeń [30], zaobserwowaliśmy całkowite wyleczenie mieszanego owrzodzenia, na które pacjent cierpiał przez rok, w dziewiątym tygodniu połączonego protokołu bez rozwoju zdarzeń niepożądanych. Należy jednak wziąć pod uwagę wpływ całego procesu opieki, ponieważ nie można oddzielnie ocenić interwencji przeprowadzonych podczas całego okresu leczenia.
Rzeczywiście, będąc pojedynczym przypadkiem, nie możemy wykluczyć, że inne czynniki mogą odgrywać rolę w leczeniu owrzodzenia żylnego, np. jakość oczyszczania i kompresji oraz przerwanie terapii steroidami.
W przyszłości zaawansowana wizualizacja pól magnetycznych i obecność fizyków w zespole medycznym może być przydatna w dogłębnym zrozumieniu interakcji fal z organizmem i osiągnięciu bardziej specyficznego podawania [42]. Rzeczywiście, interesująca byłaby ocena możliwości wykorzystania magnetoforezy (tj. zwiększenia przenikania leku przez bariery biologiczne za pomocą pola magnetycznego) do dostarczania leków miejscowych oprócz pól magnetycznych w leczeniu ran. Proces ten może wywierać wymuszające działanie w leczeniu owrzodzeń. Wykazano, że magnetoforeza zwiększa biodostępność niektórych leków przez skórę, potencjalnie poprawiając ich dostarczanie i działanie farmakologiczne [43,44]. Jednakże, zgodnie z naszą wiedzą, nie są znane żadne dodatkowe leki stosowane w terapii diamagnetycznej w leczeniu owrzodzeń. Ponadto należy rozważyć, czy pola magnetyczne mogą wywierać inny wpływ na farmakokinetykę i farmakodynamikę leków.
Podsumowując, nasz opis przypadku sugeruje, że terapia diamagnetyczna może stanowić interesującą nieinwazyjną opcję jako dodatkowe leczenie pacjentów z owrzodzeniami żylnymi. Dane przedkliniczne opisują kilka mechanizmów, dzięki którym może ona przyspieszyć procesy gojenia i promować drenaż, podczas gdy dane kliniczne są ograniczone do niepotwierdzonych doniesień i małych badań klinicznych. W celu porównania wyników i uzyskania wysokiej jakości dowodów potrzebne są większe randomizowane badania kontrolne oraz standaryzowane procedury diagnostyczne i terapeutyczne. Ponadto interakcje między polami magnetycznymi i dodatkowymi lekami wymagają dalszej analizy.
Wkład autora: Konceptualizacja, R.R. i P.R.; metodologia, G.M. i A.C.; walidacja, G.D.S., R.S. i L.G.; analiza formalna, R.R. i P.R.; dochodzenie, R.R., V.R., C.P. i L.M.; zasoby, R.C, P.R. i G.D.S.; opieka nad danymi, C.P.; pisanie - przygotowanie oryginalnej wersji roboczej, R.R.; pisanie - recenzja i edycja, P.R.; nadzór, L.G. Wszyscy autorzy przeczytali i zgodzili się na opublikowaną wersję manuskryptu.
Finansowanie: To badanie nie otrzymało żadnego zewnętrznego finansowania. Oświadczenie Institutional Review Board: Nie dotyczy. Oświadczenie o świadomej zgodzie: Nie dotyczy.
Podziękowania: Dziękujemy pacjentce za udział w tym opisie przypadku.
Konflikt interesów: Autorzy nie zgłaszają konfliktu interesów.
Department of Health Science, School of Medicine, University of Catanzaro, 88100 Catanzaro, Włochy; roberta.roberti9@outlook.com (R.R.); gianmarco.marciano@libero.it (G.M.); al.cas1993@gmail.com (A.C.); raniavincenzo1@gmail.com (V.R.); luciamuraca@libero.it (L.M.); citraro@unicz.it (R.C.);
desarro@unicz.it (G.D.S.); gallelli@unicz.it (L.G.)
2 Operative Unit of Clinical Pharmacology and Pharmacovigilance, Mater Domini Hospital, 88100 Catanzaro, Włochy; palleria@unicz.it
3 Department of Primary Care, Azienda Sanitaria Provinciale Catanzaro, 88100 Catanzaro, Włochy
4 Research Center FAS@UMG, Department of Health Science, School of Medicine, University of Catanzaro, 88100 Catanzaro, Włochy
5 Interuniversity Center of Phlebolymphology (CIFL), International Research and Educational Program in
Clinical and Experimental Biotechnology”, Department of Surgical and Medical Sciences, University Magna Graecia of Catanzaro, 88100 Catanzaro, Włochy; rserra@unicz.it
6 Wydział Nauk Medycznych i Chirurgicznych, Uniwersytet w Catanzaro, 88100 Catanzaro, Włochy
7 Department of Orthopedics, Istituto di Ricovero E Cura A Carattere Scientifico, Istituto Ortopedico Galeazzi, 20123 Mediolan, Włochy
8 Department of Health Science, School of Medicine, Medifarmagen SRL Spin Off University of Catanzaro,
88100 Catanzaro, Włochy
* Korespondencja: romeo.p@libero.it
Roberta Roberti 1, Gianmarco Marcianò 1, Alessandro Casarella 1 , Vincenzo Rania 1, Caterina Palleria 2
Lucia Muraca 1,3, Rita Citraro 1,2,4 , Giovambattista De Sarro 1,2,4, Raffaele Serra 5,6 , Pietro Romeo 7,*
Bibliografia :
1. Schneider, C.; Stratman, S.; Kirsner, R.S. Wrzody kończyn dolnych. Med Clin. N. Am. 2021, 105, 663–679. [CrossRef] [PubMed]
2. Kirsner, R.; Vivas, A. Owrzodzenia kończyn dolnych: diagnoza i leczenie. br. J. Dermatol. 2015, 173, 379–390. [Odniesienie krzyżowe]
3. Powers, J.G.; Higham, C.; Broussard, K.; Phillips, T. Gojenie się ran i leczenie ran. J. Am. Acad. Dermatol. 2016, 74, 607–625. [Odniesienie krzyżowe]
4. Harries, RL; Bosanquet, DC; Harding, K.G. Przygotowanie łożyska rany: CZAS na aktualizację. Wewnętrzne Rana J. 2016, 13 (Suppl. 3), 8–14. [CrossRef] [PubMed]
5. Gallelli, G.; Cione, E.; Serra, R.; Leo, A.; Citraro, R.; Matricardi, P.; Di Meo, C.; Bisceglia, F.; Caroleo, MC; Basile, S.; i in. Nanohydrożel z kwercetyną i kwasem oleinowym jako nowy preparat w leczeniu owrzodzeń stopy cukrzycowej: badanie pilotażowe. Wewnętrzne Rana J. 2019, 17, 485–490. [Odniesienie krzyżowe]
6. Romano, F.; Paolino, FM; Rizzo, BA; Russo, A.; Southworth, S.; Serra, R.; Gallelli, L. Zastosowanie czynników wzrostu, komórek CD34 + i fibryny w leczeniu przewlekłych owrzodzeń żylnych. Wewnętrzne Rana J. 2015, 13, 1011–1013. [Odniesienie krzyżowe]
7. Serra, R.; Gallelli, L.; Conti, A.; De Caridi, G.; Mafalda, MM; Spinelli, F.; Buffone, G.; Amato, B.; Ceglia, S.; Spaziano, G.; i in. Wpływ sulodeksydu na parametry kliniczne i molekularne u pacjentów z mieszanymi owrzodzeniami tętniczymi i żylnymi kończyn dolnych. Lek Des. Rozw. Tam. 2014, 8, 519–527. [CrossRef] [PubMed]
8. Jones, RE; Foster, DS; Longaker, MT Postępowanie w ranach przewlekłych — 2018. JAMA: J. Am. Med doc. 2018, 320, 1481–1482.
[CrossRef] [PubMed]
9. Markov, MS Terapia polem magnetycznym: recenzja. Elektromagnes. Biol. Med. 2007, 26, 1–23. [Odniesienie krzyżowe]
10. Jiao, M.; Yin, H.; Hu, J.; Xu, W.; Zhang, X.; Zhang, P. Wpływ impulsowych pól elektromagnetycznych o niskiej częstotliwości na gojenie się wrzodów stresowych na dużych wysokościach u szczurów. BioMed Res. Wewnętrzne 2019, 2019, 6354054–8. [Odniesienie krzyżowe]
11. Ross, C.L. Zastosowanie pola elektrycznego, magnetycznego i elektromagnetycznego do ukierunkowanej migracji i adhezji komórek w medycynie regeneracyjnej. Biotechnologia. Wałówka. 2017, 33, 5–16. [Odniesienie krzyżowe]
12. Albuquerque, W.; Costa, RMPB; de Salazar i Fernandes, T.; Porto, A.L.F. Dowody na wpływ statycznego pola magnetycznego na układy komórkowe. Wałówka. Biofizyka. Mol. Biol. 2016, 121, 16–28. [CrossRef] [PubMed]
13. Saliev, T.; Mustapowa, Z.; Kulsharova, G.; Bulanin, D.; Mikhalovsky, S. Terapeutyczny potencjał pól elektromagnetycznych w inżynierii tkankowej i gojeniu ran. Prolif komórkowy. 2014, 47, 485–493. [CrossRef] [PubMed]
14. Costin, G.-E.; Birlea, SA; Norris, DA Trendy w gojeniu ran: Komórkowe i molekularne podstawy terapii regeneracyjnej z wykorzystaniem pól elektromagnetycznych. Aktualny Mol. Med. 2012, 12, 14–26. [CrossRef] [PubMed]
15. Premi, E.; Benussi, A.; La Gatta, A.; Visconti, S.; Costa, A.; Gilberti, N.; Cantoni, V.; Padovani, A.; Borroni, B.; Magoni, M. Modulacja długotrwałej plastyczności korowej przypominającej wzmocnienie w zdrowym mózgu za pomocą pulsacyjnych pól elektromagnetycznych o niskiej częstotliwości. BMC Neurosci. 2018, 19, 34. [Odn.Krzyżowe]
16. Izzo, M.; Napolitano, L.; Coscia, V.; La Gatta, A.; Mariani, F.; Gasbarro, V. Rola pompy diamagnetycznej (CTU mega 18) w fizycznym leczeniu obrzęku limfatycznego kończyn. Badanie kliniczne. EUR. J. Lymphol. 2010, 21.
17. Apolone, G.; Mosconi, P. Włoskie badanie zdrowotne SF-36: tłumaczenie, walidacja i normalizacja. J. Clin. Epidemiol. 1998, 51,
1025–1036. [Odniesienie krzyżowe]
18. Hedayati, N.; Carson, JG; Chi, Y.-W.; Link, D. Postępowanie w przypadku mieszanych owrzodzeń tętniczych i żylnych kończyn dolnych: przegląd. Vasc. Med. 2015, 20, 479–486. [CrossRef] [PubMed]
19. Mallet, L.; Spinewino, A.; Huang, A. Wyzwanie związane z zarządzaniem interakcjami leków u osób starszych. Lancet 2007, 370, 185–191. [Odniesienie krzyżowe]
20. Gallelli, L.; Siniscalchi, A.; Palleria, C.; Mumoli, L.; Staltari, O.; Squillace, A.; Maida, F.; Russo, E.; Gratteri, S.; De Sarro, G.; i in. Działania niepożądane leków związane z podawaniem leków u pacjentów hospitalizowanych. Aktualny Bezpieczny lek. 2017, 12, 171–177. [Odniesienie krzyżowe]
21. O’Meara, S.; Cullum, N.; Nelson, EA; Dumville, J.C. Kompresja na żylne owrzodzenia podudzi. System baz danych Cochrane Rev. 2012, 2012,
CD000265. [CrossRef] [PubMed]
22. Mosti, G.; Iabichella, ML; Partsch, H. Terapia uciskowa w mieszanych owrzodzeniach zwiększa pojemność żylną i perfuzję tętniczą. J. Vasc. Surg. 2012, 55, 122–128. [CrossRef] [PubMed]
23. Kranke, P.; Bennett, MH; James, MM-S; Schnabel, A.; Debus, SE; Weibel, S. Hiperbaryczna terapia tlenowa ran przewlekłych.
System baz danych Cochrane Wersja 2015, 2015, CD004123. [Odniesienie krzyżowe]
24. Mert, T.; Yaman, S. Prozapalne lub przeciwzapalne działanie zabiegów pulsacyjnym polem magnetycznym u szczurów z eksperymentalnym ostrym zapaleniem. Otaczać. Nauka. Zanieczyszczać. Rozdzielczość 2020, 27, 31543–31554. [Odniesienie krzyżowe]
25. Purnell, MC; Skrinjar, T.J. Dielektroforetyczna dysocjacja jonów chlorkowych i wpływ na anizotropię diamagnetyczną w błonach komórkowych. Odkryć Med. 2016, 22, 257–273.
26. Smith, T.L.; Wong-Gibbons, D.; Maultsby, J. Mikrokrążeniowe skutki pulsacyjnych pól elektromagnetycznych. J. Orthop. Rozdzielczość 2004, 22,
80–84. [Odniesienie krzyżowe]
27. Bragin, DE; Statom, GL; Hagberg, S.; Nemoto, E.M. Zwiększa perfuzję mikronaczyń i natlenienie tkanek poprzez pulsacyjne pola elektromagnetyczne w mózgu zdrowego szczura. J. Neurochirurg. 2015, 122, 1239–1247. [Odniesienie krzyżowe]
28. Callaghan, M.J.; Chang, EI; Seiser, N.; Aarabi, S.; Ghali, S.; Kinnucan, ER; Simon, BJ; Gurtner, G.C. Pulsacyjne pola elektromagnetyczne przyspieszają gojenie ran normalnych i cukrzycowych poprzez zwiększenie uwalniania endogennego FGF-2. Plastik. Rekonstrukcja Surg. 2008, 121, 130–141. [Odniesienie krzyżowe]
29. Lee, RC; Canaday, DJ; Doong, H. Przegląd biofizycznych podstaw klinicznego zastosowania pól elektrycznych w naprawie tkanek miękkich. J. Burn. Opieka Rehabilitacyjna. 1993, 14, 319–335. [Odniesienie krzyżowe]
30. Aziz, Z.; Cullum, N. Terapia elektromagnetyczna w leczeniu owrzodzeń żylnych podudzi. System baz danych Cochrane Wersja 2015, 2015, CD002933.
[CrossRef] [PubMed]
31. Markoll, R.; Ferreira, DMDS; Toohil, T.K. Pulsed Signal Therapy®: przegląd. APLAR J. Rheumatol. 2003, 6, 89–100. [Odniesienie krzyżowe]
32. Gill, SE; Parki, WC Metaloproteinazy i ich inhibitory: regulatory gojenia ran. Wewnętrzne J. Biochem. Biol Komórkowy. 2008, 40, 1334–1347. [Odniesienie krzyżowe]
33. Gordon, GA Zaprojektowana terapia impulsami elektromagnetycznymi: zastosowania kliniczne. J. Cell. Fizjol. 2007, 212, 579–582. [Odniesienie krzyżowe]
34. Dunnill, C.; Pattona, T.; Brennan, J.; Barrett, J.; Dryden, M.; Cooke, J.; Leaper, D.; Georgopoulos, NT Reaktywne formy tlenu (ROS) i gojenie się ran: funkcjonalna rola RFT i nowych technologii modulujących ROS w celu wspomagania procesu gojenia. Wewnętrzne Rana J. 2017, 14, 89–96. [Odniesienie krzyżowe]
35. Strauch, B.; Patel, MK; Navarro, JA; Berdyczewski, M.; Yu, H.-L.; Pilla, AA Pulsacyjne pola magnetyczne przyspieszają gojenie się ran skórnych u szczurów. Plastik. Rekonstrukcja Surg. 2007, 120, 425–430. [CrossRef] [PubMed]
36. Detlavs, I.; Dombrowska, L.; Turauska, A.; Shkirmante, B.; Słuckij, L. Eksperymentalne badanie wpływu pól elektromagnetycznych o częstotliwości radiowej na zwierzęta z ranami tkanek miękkich. Nauka. Całkowite środowisko. 1996, 180, 35–42. [Odniesienie krzyżowe]
37. Ieran, M.; Zaffuto, S.; Bagnacani, M.; Annovi, M.; Moratti, A.; Cadossi, R. Wpływ pulsujących pól elektromagnetycznych o niskiej częstotliwości na owrzodzenia skóry pochodzenia żylnego u ludzi: badanie z podwójnie ślepą próbą. J. Orthop. Rozdzielczość 1990, 8, 276–282. [Odniesienie krzyżowe]
38. Stiller, M.; Pak, GH; Shupack, J.; Talar, S.; Kenny, C.; Jondreau, L. Przenośne urządzenie z pulsacyjnym polem elektromagnetycznym (PEMF) wspomagające gojenie opornych owrzodzeń żylnych: badanie kliniczne z podwójnie ślepą próbą, kontrolowane placebo. br. J. Dermatol. 1992, 127, 147–154. [Odniesienie krzyżowe]
39. Kenkre, J.; Hobbs, R.; Carter, Y.; Holder, R.; Holmes, E. Randomizowana, kontrolowana próba terapii elektromagnetycznej w leczeniu podstawowej opieki zdrowotnej w przypadku owrzodzeń żylnych podudzi. Rodzina. Pr. 1996, 13, 236–241. [CrossRef] [PubMed]
40. Pasek J.; Cieślelar, G.; Sieron´, A. Terapia skojarzona w leczeniu owrzodzeń podudzi o mieszanej etiologii – opis przypadku. Tam. Clin. Zarządzanie ryzykiem 2018, ume 14, 1915–1921. [Odniesienie krzyżowe]
41. Lv, H.; Liu, J.; Zhen, C.; Wang, Y.; Wei, Y.; Ren, W.; Shang, P. Pola magnetyczne jako potencjalna terapia ran cukrzycowych na podstawie eksperymentów na zwierzętach i badań klinicznych. Prolif komórkowy. 2021, 54, e12982. [CrossRef] [PubMed]
42. Zborowski, M.; Midura, RJ; Wolfman, A.; Patterson, T.; Ibiwoye, M.; Sakai, Y.; Grabiner, M. Wizualizacja pola magnetycznego w zastosowaniach do stymulacji tkanek pulsacyjnym polem elektromagnetycznym. Anna. Biomed. inż. 2003, 31, 195–206. [Odniesienie krzyżowe]
43. Raghu, PK; Bansal, K.K.; Thakor, P.; Bhavana, V.; Madan, J.; Rosenholm, JM; Mehra, N.K. Ewolucja nanotechnologii w dostarczaniu leków do oczu, skóry i ran drogą miejscową. Farmaceutyka 2020, 13, 167. [CrossRef]
44. Murthy, SN; Sammeta, SM; Bowers, C. Magnetoforeza w celu zwiększenia przezskórnego dostarczania leków: badania mechaniczne i projektowanie plastrów. J. Kontrola. Wydanie 2010, 148, 197–203. [CrossRef] [PubMed]